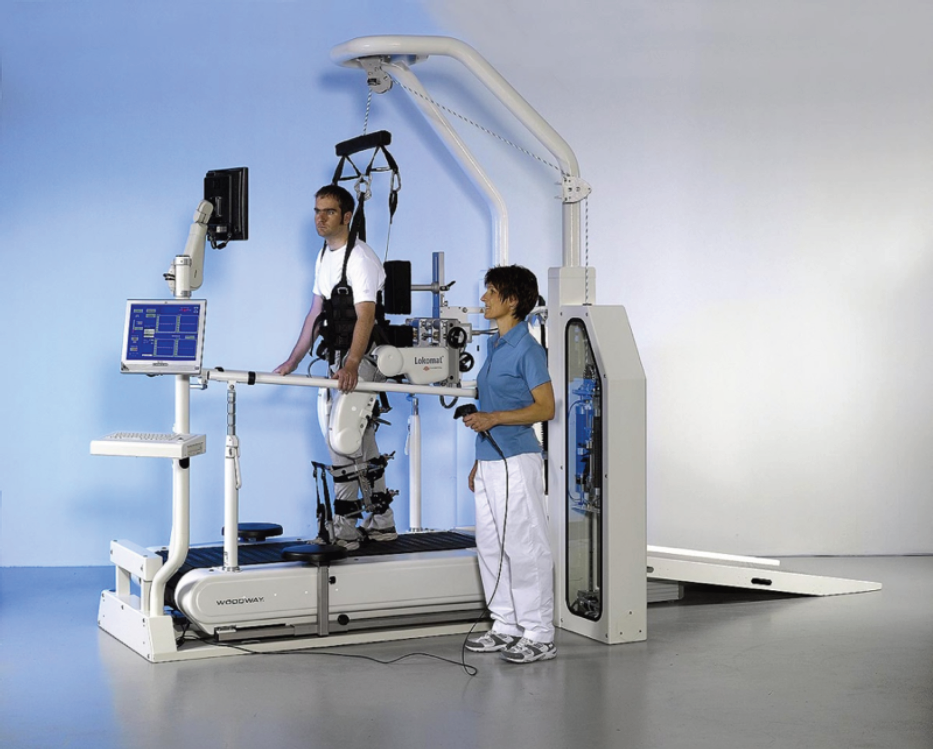
Los pacientes pudieron dar sus primeros pasos una hora después de que los neurocirujanos les implantaron por primera vez prototipos de un dispositivo de estimulación nerviosa controlado a distancia por un software de inteligencia artificial.
En los seis meses siguientes, los pacientes recuperaron la capacidad de realizar actividades más avanzadas -caminar, montar en bicicleta y nadar en entornos comunitarios fuera de la clínica- controlando ellos mismos los dispositivos de estimulación nerviosa mediante una tableta con pantalla táctil, explicaron los investigadores.
Los pacientes, hombres de 29, 32 y 41 años, sufrieron lesiones en accidentes de moto.
La empresa espera poner en marcha una prueba dentro de un año en la que participen entre 70 y 100 pacientes, principalmente en Estados Unidos, explicó Courtine.
Si los primeros resultados de este estudio se confirman en otros más amplios, las personas inmovilizadas por lesiones de la médula espinal podrían algún día abrir un teléfono inteligente o hablar con un reloj inteligente, seleccionar una actividad como “caminar” o “sentarse”, y luego enviar un mensaje a un dispositivo implantado que estimulará nervios y músculos para que se realicen los movimientos, dijeron los investigadores.
Normalmente, para iniciar el movimiento, el cerebro envía un mensaje a la médula espinal, indicándole que estimule un conjunto de células nerviosas que, a su vez, activan los músculos necesarios, explicó Bloch.
“Es algo en lo que ni siquiera pensamos”, dijo Bloch. “Se produce automáticamente”. Tras una lesión completa de la médula espinal, los mensajes del cerebro no pueden llegar a los nervios.
Otros investigadores han tratado de ayudar a los pacientes paralizados a caminar estimulando los nervios a través de la parte posterior de la columna vertebral, usando campos eléctricos emitidos por dispositivos implantados y originalmente diseñados para controlar el dolor crónico, dijo Courtine.
Courtine y Bloch y su equipo rediseñaron los dispositivos para que las señales eléctricas entraran en la columna vertebral por los lados en lugar de por la espalda. Este enfoque permite dirigir y activar de forma muy específica las regiones de la médula espinal, explicó Courtine.
A continuación, idearon algoritmos de inteligencia artificial que ordenan a los electrodos del dispositivo que emitan señales para estimular, en la secuencia adecuada, los nervios individuales que controlan los músculos del tronco y las piernas necesarios para diversas actividades, como levantarse de una silla, sentarse y caminar.
El software se adapta a la anatomía de cada paciente, manifestó Courtine.
Cuando se implantó el dispositivo, los pacientes podían “activar inmediatamente las piernas y pisar”, dijo Bloch.
Pero como sus músculos estaban debilitados por el desuso, necesitaron ayuda para soportar el peso y tuvieron que aprender a trabajar con la tecnología, dijeron los investigadores.
Los investigadores señalaron que, aunque los pacientes recuperaron la capacidad de realizar diversas actividades, incluido el control de los músculos del tronco, durante “amplios periodos”, no recuperaron los movimientos naturales.
Aun así, Bloch dijo: “Cuanto más se entrenen, cuanto más empiecen a levantar los músculos, más fluido será”.
Estudio sobre el ratón
Otro artículo revisado por un equipo de investigación distinto en Israel, publicado el lunes en la revista Advanced Science, describe un enfoque experimental para reparar las lesiones de la médula espinal.
Los investigadores de la Universidad de Tel Aviv intentaron reparar las médulas espinales de ratones lesionados usando células humanas adultas que habían sido diseñadas para comportarse como células madre embrionarias, que pueden convertirse en cualquier tipo de célula del cuerpo.
Las médulas espinales de los animales habían formado tejido cicatricial, lo que ha impedido cualquier beneficio de dichas células en estudios anteriores.
Los investigadores permitieron primero que las células madre florecieran en un entorno especial de tubo de ensayo, y sólo las trasplantaron a los ratones una vez que las células habían madurado en una pequeña red de células nerviosas y después de haber eliminado quirúrgicamente el tejido cicatricial
Los investigadores informaron que habían logrado un 80% de éxito en la restauración del movimiento y la sensibilidad de los ratones paralizados. Los investigadores afirmaron que pretenden hacer pruebas en humanos dentro de unos años.
Los esfuerzos por utilizar este tipo de células madre para ayudar a la columna vertebral a repararse a sí misma y restaurar la función de órganos y extremidades aún no han producido un tratamiento aprobado en humanos.
“Queda un largo camino para demostrar que también funciona en humanos, pero ese es nuestro objetivo”, dijo Tal Dvir, que dirigió el equipo del Centro Sagol de Biotecnología Regenerativa.